基因治疗小圆桌:重组腺相关病毒载体相关性杂质
点击蓝字
关注我们
”
rAAV优点
重组腺相关病毒载体(rAAV)与其他病毒载体相比,具有安全性好、宿主细胞范围广、免疫源性低、转染效率高、非致病性、在体内表达外源基因时间长等优点,已成为体内基因治疗的主要病毒载体之一,在世界范围内的基因治疗和疫苗研究中得到广泛应用。
rAAV 载体相关性杂质有哪些?
rAAV 载体相关性杂质是指与其本身性质非常类似的杂质,主要包括3类:包裹有载体基因组之外的核酸序列的类 AAV 病毒颗粒;空病毒颗粒;rAAV 多聚体。
rAAV 载体相关性杂质危害?
类 AAV 病毒颗粒中包装的抗生素抗性序列可能会引起病人对抗生素的耐药性,AAV 复制基因 rep 则具有潜在的致突变风险;空病毒颗粒内不含转基因组,会增加抗原输入量,另外会降低 rAAV 载体的溶解度,促进其凝聚,影响其储存稳定性;rAAV 多聚体的形成则会严重降低产品的稳定性,增加衣壳抗原的免疫原性。
如何减少 rAAV 载体相关杂质的污染?
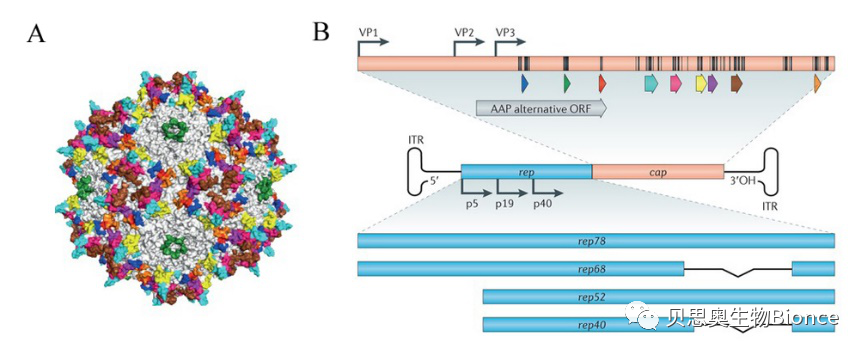
防止 rAAV 载体相关杂质的形成,是当前建立 rAAV 载体生产工艺最重要的任务之一,具体有以下方法:
1
减少类 AAV 病毒颗粒污染
在生产 rAAV 载体的过程中,转染用质粒或宿主细胞 DNA 会被误包装而形成类 AAV 病毒颗粒。类 AAV 病毒颗粒又可分为可复制型 (rcAAV) 和复制缺陷型两类。因类 AAV 病毒颗粒与真正的 AAV 病毒几乎完全一样,一旦形成则难以去除,必须从包装工艺入手防止或减少其产生。
类AAV 病毒颗粒的形成主要是由于 rAAV 载体质粒和辅助质粒间的非同源重组而引起,载体质粒中含有的 ITR 在重组事件中发挥了重要作用,将载体质粒中 ITR 的 D 序列远端的 10 个核苷酸缺失,可以抑制载体质粒和辅助质粒之间的非同源重组,产品中 rcAAV 的含量因此大大降低。
将位于rep 基因 5′端的顺式复制元件 (CARE)缺失,可有效控制包装有 rep-cap 基因的复制缺陷型类 AAV 病毒颗粒的产生。将rep和cap基因分为两个独立的转录单元,且转录方向相反,可有效地降低rep和cap基因被重组包装为 rcAAV 的可能性。
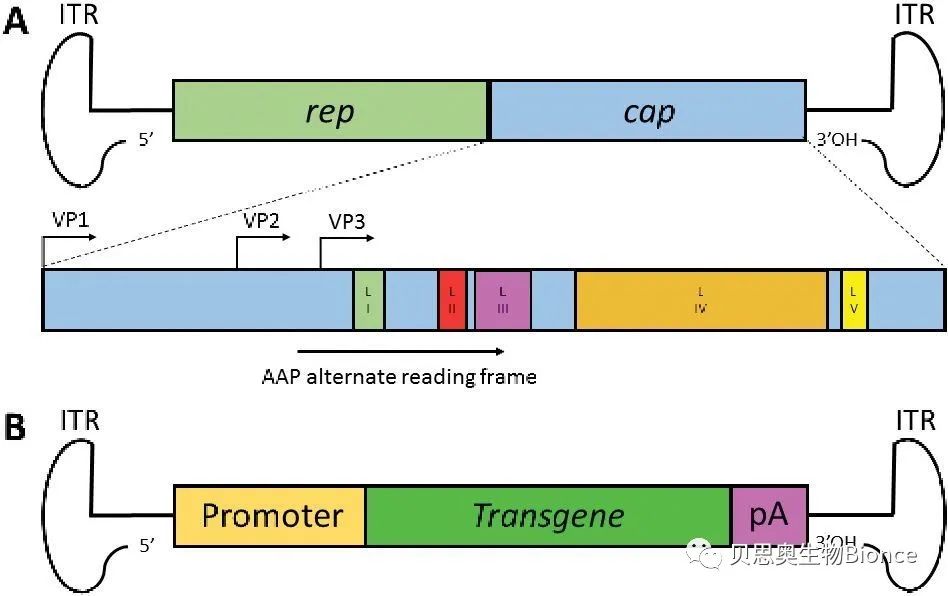
在辅助质粒的rep和cap表达框内插入某些特定的内含子,使得辅助质粒基因组的大小远远超出 AAV 的包装容量而不被误包装,rcAAV 的污染可以降低 2~3 个数量级。
2
减少空病毒颗粒污染
AAV 空病毒颗粒是不含任何 DNA 的假病毒,仅由 3 种不同的衣壳蛋白 VP1、VP2 和 VP3 组成,构成定量比与真 AAV 一样为 1∶1∶10。空病毒颗粒的自组装与载体 DNA 的复制和包装无关。rAAV 载体衣壳与 AAV 空病毒颗粒的构成完全一致,采用实验室常规的亲和层析方法根本不能将二者有效分离。
由于空病毒颗粒与 rAAV 载体浮力密度的差异,可以通过密度梯度离心法进行分离,该方法适用于所有血清型rAAV 的纯化。但是仅经密度梯度离心得到的产品,纯度尚达不到临床应用标准,另外处理量小、不易放大生产规模也限制了其应用。目前常用切向流过滤(TFF) 技术,对密度梯度离心前样品进行浓缩,浓缩样品经碘克沙醇密度梯度离心得到的 rAAV8、rAAV9 载体产品中,空白病毒颗粒含量为 0.4%~5%。
采用阴离子交换色谱可以将空病毒颗粒与 rAAV1 载体有效分离。经过 1 次高分辨柱阴离子交换色谱分离后,大约 90%的空病毒颗粒被去除。第 2 次高分辨柱纯化后得到的 rAAV1 载体样品中空病毒颗粒含量少于 5%,回收率均高于50%。采用阳离子和阴离子交换二步色谱法,得到的终产品中空病毒颗粒含量小于1%,总体收率为74%。该工艺不仅适用于血清型rAAV2 载体,也可以用于rAAV6 载体的纯化。
膜色谱是将液相色谱与膜分离融合于一起的新型生化分离技术,具有选择性高、分离速度快、能耗低、易放大等特点,是分离纯化生化大分子药物的有力工具。将rAAV 载体收获液上样至阳离子交换膜后,空病毒颗粒因等电点高呈现较强的正电性,绝大部分 (97%)被吸附至阳离子交换膜,而 rAAV 载体则直接穿透通过。然后将穿透液上样至阴离子交换膜,经 NaCl浓度线性洗脱后,空病毒颗粒含量降低至 1%以下。
3
减少rAAV 多聚体污染
rAAV 载体的纯化和储存过程中,如实验条件选择不当,往往会促使 rAAV 载体聚集形成多聚体,从而影响纯化收率,降低产品的稳定性。
小结
参考文献:刁勇. 重组腺相关病毒载体相关性杂质[J]. 生物工程学报, 2011, 27(5):717-723.
“
关于我们
南京贝思奥 (BIONCE) 生物科技有限公司成立于2020年,公司致力于基于重组病毒的基因治疗药物的研发、生产与质量控制,并研制具有自主知识产权的临床基因治疗药物。主要用于治疗眼科疾病、神经系统疾病、恶性肿瘤、罕见病等,打造基因治疗技术研发创新基地。

“

”
关注我们