基因治疗小圆桌:生物制品细菌内毒素检测方法简介

背景
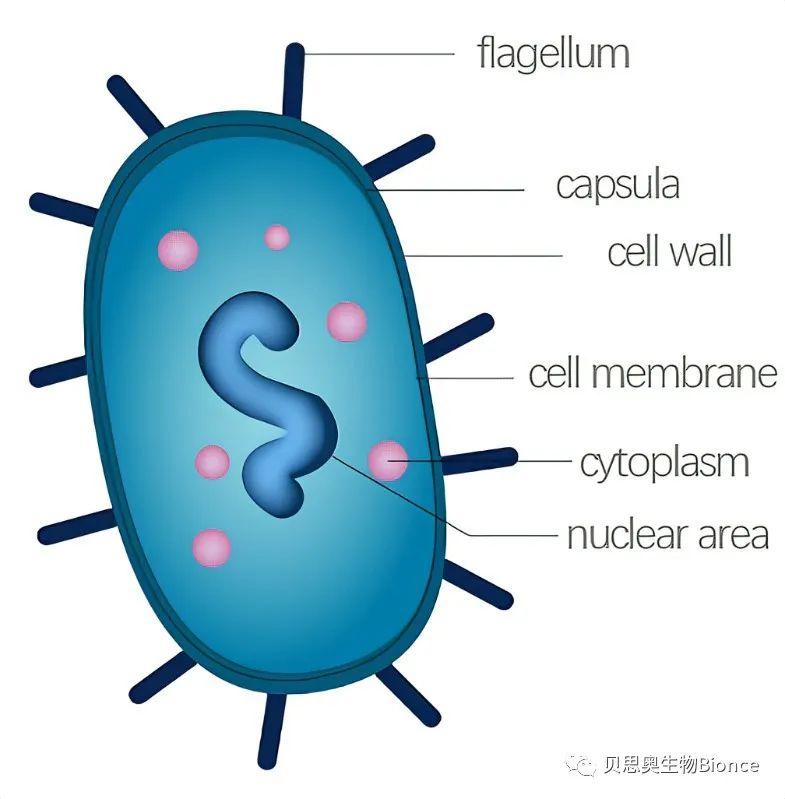
细菌内毒素,进入血液或脑脊液时会引起发热,因此,又称为“热原”,它是革兰氏阴性菌细胞壁上的特有结构,细菌在存活状态时不释放出来,只有当细菌死亡自溶时才释放到细胞外,表现多种毒性作用,为区别于外毒素而称之为内毒素。细菌内毒素作为外源性致热原,极微量即可对人体健康产生严重影响,能引起发热、微循环障碍、内毒素血症、内毒素休克和弥散性血管内凝血等,严重者会造成死亡。因此,对生物制品进行内毒素检测至关重要。
一
细菌内毒素检测


传统方法
1.兔子热原测试(RPT)
家兔对热原的反应与人基本相似,因此采用家兔耳静脉注射的方式,在规定时间内通过监测家兔体温,来定性检测热原,兔子热原测试是一种更具侵入性的检测样本中热原存在的方法,也是检测内毒素的第一种标准方法。
兔热原试验是FDA批准的检测热原的方法,不仅包括内毒素,还包括非内毒素。这是一种检测热原的简单方法,制药公司在发布产品之前通常使用这种方法。但是此方法存在检测结果不能定量、检测周期长、灵敏度低等缺点。
2.鲎试剂检测法(limulusamoebocytelysatetest,LAL)
LAL主要分为两大类:凝胶法和光度测量法。
凝胶法
凝胶法是通过鲎试剂与内毒素产生凝集反应的原理进行半定量检测内毒素的方法,由于其是基于鲎试剂中多个酶蛋白在模拟的生理环境下进行的反应,在反应过程中会受到很多生化因素的影响。此外,由于内毒素本身的特性,易造成吸附和聚集,在反应过程中,易造成假阳性或假阴性结果。因此,消除干扰因素影响对LAL检测内毒素尤为必要。此检测方法虽为内毒素检测的标准方法,但检测范围存在一定的局限性,且对检测用水和检测条件均存在一定的要求。
光度测量法
光度法(包括浊度法和显色法)可定量检测内毒素的含量,其中浊度法是通过内毒素与鲎试剂的C因子产生反应,由此激活的凝固酶会切断凝固蛋白原中的精氨酸肽链,形成凝胶状蛋白;而显色基质法是通过测定内毒素与鲎试剂反应时产生的凝固酶使某种特殊底物释放出来的生色团的量,来检测内毒素含量的鲎试验法。此方法能较为准确评估产品在生产过程中污染的相对风险,定量检测的数据不仅有利于追踪产品质量趋势,还能起到风险预警的作用,达到数据完整性的要求。
光度法的检测范围比凝胶法宽,使得有干扰的样品可以有更大的稀释倍数,对于部分使用凝胶法无法排除干扰的样品,可以尝试使用光度法建立细菌内毒素检测方法。
传
统
方
法

新型方法
1.免疫学方法
ELISA法是目前新兴的内毒素检测方法,它是基于抗原抗体的酶联免疫测定法,由于兼具抗原抗体反应的高特异性和酶的高效催化作用而被应用于内毒素的检测,近年来得到了广泛的发展和应用。目前常用的内毒素检测的免疫学方法包括 L⁃聚赖氨酸 ELISA法、火箭免疫电泳鲎试验法和双抗体夹心 ELISA 法等。免疫法测定内毒素具有较高的特异性,但易受外界环境的影响,在高温、强酸、强碱等检测环境中易变性,使实验结果出现假阳性,且实验时间相对较长。
2. 重组 C 因子法
重组 C 因子是一种人工克隆的C 因子,与 C 因子具有一样的生理活性,经内毒素活化后,可与荧光底物作用产生荧光复合物,通过检测荧光信号进而实现对内毒素的定量检测。此方法为一步反应,激活的C因子可直接剪切荧光底物,有效避免干扰,提高实验结果的准确性,具有可靠的特异性和一致性,并且无动物来源。目前,FDA现已批准重组C因子作为鲎试剂的替代方案,用于生物制品的放行和过程检测。2020版中国药典通则9301附录里面也有关于重组C因子的检测说明,但是如需放行检测,还需要做相关验证试验。
3.单核细胞活化反应测定法(monocyte activationtest,MAT)
该方法利用单核细胞或单核细胞系模拟人体,以LPS标准品为基准做线性回归,检测并比较由标准品和供试品分别刺激单核细胞所产生的活化反应,通过测定释放促炎症细胞因子的量来判定供试品中内毒素含量。MAT可同时检测药品和医疗器械等注射用品中的内毒素和非内毒素热原,而且被2010版欧洲药典采纳,取代家兔热原试验成为新的药典方法,FDA行业指南同样也提及这一检测法。
单核细胞激活试验 (MAT) 有助于检测和量化激活人类单核细胞以释放负责发烧反应的介质的物质,不仅可以确定内毒素热原,还可以帮助确定非内毒素热原。
4.生物传感器检测法
生物传感器指以具有生物识别作用的生物成分或生物体本身为敏感材料,与适当的信号转换器相结合,将生化反应的程度用离散或连续的信号表达出来,从而能进行生命物质和化学物质检测及监控的装置。生物传感器由于具有测量速度快、敏感性高、最低检测限低等优点,近年来已被广泛应用于各领域,在内毒素检测方面也得到了广阔的发展,为替换传统的内毒素检测方法提供了新的思路。
新
型
方
法
二
细菌内毒素污染的控制

内毒素对热的耐受性非常强。常用的湿热灭菌法(121 ℃,1 h)不能破坏内毒素。破坏内毒素生物活性的最有效方法是干热灭菌法。一般180 ℃ 3~4 h、200 ℃ 60 min或250℃ 30~45min,或用强碱强酸才能彻底破坏它。
生物制品中内毒素的来源主要有:菌毒种、生产环境、不规范操作、设备及器械、原辅材料等。对于生物制品生产中内毒素污染的控制最主要的措施是生产过程控制,即严格按GMP要求进行生产,严格无菌操作,防止内毒素产生。
三
细菌内毒素去除

细菌内毒素的去除可采用亲合层析、离子交换层析、疏水层析、分子筛层析、超滤法、吸附法等。
亲合层析:亲合层析技术,特别是免疫吸附剂在生产中的运用使得生物大分子的纯化变得简单。选择性内毒素去除填料是一种以形成共价键的方式,将安全性高的内毒素类似底物固定至纤维素微粒的新型内毒素除去剂。可在生理pH值,温度0 ℃-25 ℃的条件下去除内毒素。该填料刚性更好,特异性更强,样品回收率更高。
离子交换层析:是通过带电溶质分子与离子交换剂中可交换的离子进行交换而进行纯化的方法。内毒素在pH>2时带负电荷,与阴离子交换介质Q或DEAE基团有较强结合,可在目标物流穿或洗脱后,用高盐缓冲液或NaOH去除,这是离子交换法去除内毒素的基础。
超滤法:超滤法是基于分子量的大小去除内毒素,适用于水溶液和小分子溶液去除内毒素,在蛋白质等大分子物质使用超滤法会导致有效分子大量流失。但由于膜吸附过程中产热及系统残留等原因,活性损失较大。
四
小结

内毒素对生物制品的危害虽然很严重,但只要我们了解了内毒素的特性,就可以采取适合自己的有效方法加以控制和去除。内毒素普遍存在于生活中,适量的内毒素可促进细胞因子激活免疫系统,对机体有益,而过量则可引起机体严重的病理反应,所以注射制剂中内毒素的检测和控制显得尤为重要。
目前鲎试剂法以灵敏度高、操作简易而最常用,但是随着环境的恶化以及过度捕杀,中华鲎和圆尾鲎已经成为濒危生物,所以急需内毒素检测代替方法进行弥补。随着研究的不断深入,细菌内毒素检测的新方法不断被开发出来。其中重组C因子法可通过荧光信号定量检测细菌内毒素,并可有效避免其他因素干扰,将成为短期内最有望替代传统 LAL 的新型检测方法。而生物传感器检测法则代表了内毒素检测技术未来发展的趋势,目前对细菌内毒素生物传感器的研究仍处于初级阶段,还有很多问题亟待解决,想使生物传感器检测法得到更广泛的发展,需对内毒素的生物学机制进行进一步的研究和探索,以便构建更精准的生物传感器检测法。
参考文献:
[1]张媛,孙述学.细菌内毒素检测方法的研究进展[J].中国生物制品学杂志,2023,36(03):368-372+378.DOI:10.13200/j.cnki.cjb.003846.
[2]李生军,张海霞,冯若飞.生物制品中内毒素的危害及其去除方法的研究进展[J].浙江农业科学,2021,62(09):1882-1885.DOI:10.16178/j.issn.0528-9017.20210958.
长
按
BIONCE_BIOTECH
扫
码

News.
行业资讯

